مرحبًا يا من هناك! كمورد للأدوية المضادة Deruxtecan المترافق ، أنا متحمس للغاية لنأخذك في رحلة عبر تاريخ تطويرها. دعنا نغوص في!
بدايات مبكرة من الأجسام المضادة - الأدوية المترافق
الأجسام المضادة - الأدوية المترافق (ADCs) كانت موجودة لفترة من الوقت. يعود المفهوم إلى أوائل القرن العشرين. توصل بول إيرليتش ، وهو عالم ألماني ، إلى فكرة "الرصاصة السحرية" في عام 1906. لقد تصور دواءًا يمكن أن يستهدف الخلايا المريضة على وجه التحديد مع تركها صحية دون أن يصاب بأذى. كانت هذه هي الشرارة التي أشعلت الأبحاث الطويلة على المدى إلى ADC.
في العقود التالية ، كان العلماء يحاولون معرفة كيفية إرفاق عامل سام للخلايا بجسم مضاد. لكن الأمر لم يكن سهلاً. واجهوا العديد من التحديات ، مثل العثور على الأجسام المضادة الصحيحة التي يمكن أن تستهدف بدقة الخلايا السرطانية واختيار الحمولات السامة للخلايا المناسبة التي كانت قوية بما يكفي لقتل الخلايا المستهدفة.
الأول - جيل ADCs
ظهر الجيل الأول من ADCs في التسعينيات. تم تصميم هذه ADCs المبكرة لعلاج السرطان. كانت الفكرة بسيطة لكنها ثورية: استخدم جسمًا مضادًا لتقديم دواء سام للخلايا مباشرة إلى الخلايا السرطانية. واحدة من أولى ADCs المعتمدة كانت Gemtuzumab Ozogamicin في عام 2000. وقد استهدف CD33 ، وهو بروتين موجود على سطح خلايا سرطان الدم ، ويستخدمالعامل السام للورم في Calicheamicinكما الحمولة.
ومع ذلك ، كان لدى الجيل الأول ADCs بعض العيوب الرئيسية. لم تكن طرق الاقتران مستقرة للغاية ، مما يعني أن الحمولة النافعة يمكن أن تنفصل عن الجسم المضاد قبل الوصول إلى الخلايا المستهدفة. أيضا ، فإن الأجسام المضادة المستخدمة في بعض الأحيان تفتقر إلى الخصوصية ، مما يؤدي إلى التأثيرات المستهدفة والتأثيرات الجانبية في المرضى.
الثاني - جيل ADCs
مع مرور عام 2000 ، تعلم الباحثون من أخطاء الجيل الأول وبدأوا في تطوير ADC في الجيل الثاني. ركزوا على تحسين تكنولوجيا الاقتران لجعلها أكثر استقرارًا. تم تطوير تقنيات Linker الجديدة التي يمكن أن تبقي الحمولة النافعة متصلة بالأجسام المضادة حتى تصل إلى الخلايا المستهدفة.
وكان تحسن آخر في اختيار الأجسام المضادة. تمكن العلماء من تحديد الأجسام المضادة الأكثر تحديدًا التي يمكن أن تميز بشكل أفضل بين الخلايا السرطانية والخلايا الطبيعية. على سبيل المثال ، Brentuximab Vedotin ، المعتمد في عام 2011 ، يستهدف CD30 ، وهو بروتين معبر عنه على سرطان الغدد الليمفاوية هودجكين وخلايا سرطان الغدد اللمفاوية الخلوية الكبيرة. استخدمت monomethyl auristatin e (MMAE) كحمولة ، والتي تم تسليمها بشكل أكثر فعالية بسبب تقنيات الاقتران الأفضل. يمكنك معرفة المزيد عن الحمولات المماثلة مثلVal - CIT - PAB - MMAE هو مثبط مقترن للأدوية المضادة.
صعود Deruxtecan ADCs
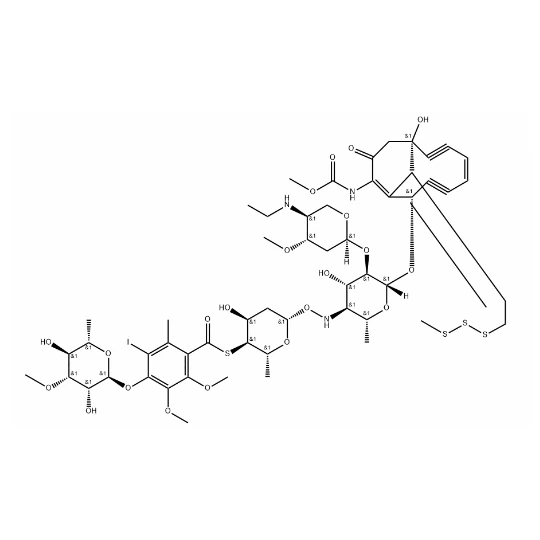
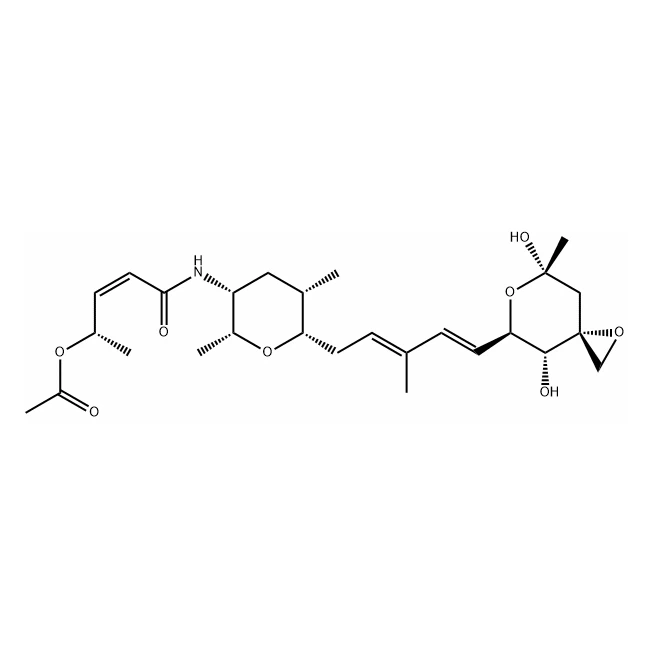
الآن ، دعنا نتحدث عن Deruxtecan ADCs. هذه هي جزء من الموجة التالية من تطوير ADC. Deruxtecan هو حمولة جديدة تحتوي على بعض الميزات الرائعة حقًا. إنه مثبط Topoisomerase I ، مما يعني أنه يمكن أن يمنع إنزيمًا أن الخلايا السرطانية تحتاج إلى تكرار الحمض النووي الخاص بها. هذا يجعله عامل سام للخلايا قوي للغاية.
بدأ تطوير ADCs المستندة إلى Deruxtecan بهدف تحسين فعالية وسلامة علاج السرطان. أراد العلماء إنشاء ADC يمكن أن يقدم حمولة Deruxtecan خصيصًا للخلايا السرطانية ، مما يقلل من الأضرار التي لحقت الأنسجة الصحية.
واحدة من أكثر deruxtecan المعروفة ADCs المعروفة هي Texertu (trastuzumab deruxtecan). إنه يستهدف HER2 ، وهو بروتين يتم التعبير عنه بشكل مفرط في بعض أنواع سرطان الثدي وسرطان المعدة وغيرها من الأورام الصلبة. جزء الأجسام المضادة من Texertu هو trastuzumab ، وهو بالفعل الجسم المضاد المضاد لـ HER2. من خلال توصيل deruxtecan إلى trastuzumab ، يمكن لـ Texertu تقديم الحمولة القوية مباشرة إلى HER2 - الخلايا السرطانية الإيجابية.
أظهرت التجارب السريرية لـ Texertu بعض النتائج المذهلة. في مرضى سرطان الثدي الذين يعانون من HER2 - مرض النقيلي الإيجابي ، أظهر TENTERU معدلات استجابة عالية وتحسينات كبيرة في التقدم - البقاء على قيد الحياة الحرة مقارنة بالعلاج الكيميائي التقليدي. هذه النتائج كانت لعبة - تغيير في مجال علم الأورام.
كيف تعمل Deruxtecan ADCs
دعنا نتفكك كيف تعمل Deruxtecan ADC على المستوى الخلوي. أولاً ، يرتبط جزء الجسم المضاد من ADC بالمستضد المستهدف على سطح الخلايا السرطانية. بمجرد الالتزام ، يتم أخذ مجمع ADC - المستضد في الخلية من خلال عملية تسمى endocytosis.
داخل الخلية ، يتم تشكيل الرابط بين الجسم المضاد وحمولة deruxtecan. هذا يطلق deruxtecan في الخلية. كما ذكرنا سابقًا ، يمنع Deruxtecan بعد ذلك topoisomerase I ، مما يمنع الخلايا السرطانية من تكرار الحمض النووي الخاص بها. بدون القدرة على تكرار الحمض النووي الخاص بهم ، لا يمكن للخلايا السرطانية أن تقسم وتموت في النهاية.
آفاق مستقبلية لـ Deruxtecan ADCs
المستقبل يبدو مشرقا ل deruxtecan ADCs. هناك جهود بحثية مستمرة لتوسيع استخدامها لأنواع أخرى من السرطان. يبحث العلماء أيضًا في طرق لتحسين التكنولوجيا بشكل أكبر. على سبيل المثال ، يستكشفون الأجسام المضادة الجديدة التي يمكن أن تستهدف أنواعًا مختلفة من السرطان - مستضدات محددة وتقنيات رابط جديدة يمكن أن تجعل ADCs أكثر استقرارًا.
مجال آخر من الأبحاث هو العلاج المركب. إن الجمع بين Deruxtecan ADC وعلاجات السرطان الأخرى ، مثل العلاج المناعي أو العلاج المستهدف ، يمكن أن يعزز تأثير مضاد للسرطان ويتغلب على مقاومة الأدوية.
لماذا نختار أدوية الأجسام المضادة Deruxtecan الخاصة بنا
كمورد للأدوية المقترنة من الجسم المضاد Deruxtecan ، فإننا نفخر بتقديم منتجات عالية الجودة. يتم تصنيع ADC لدينا باستخدام أحدث التقنيات لضمان الاستقرار والفعالية. لدينا فريق من الخبراء الذين يعملون باستمرار على تحسين منتجاتنا وضمان تلبية أعلى معايير الجودة.
إذا كنت في صناعة الأدوية ، سواء كنت باحثًا أو طبيبًا أو شركة أدوية تبحث عن علاجات سرطان مبتكرة ، فقد تكون Deruxtecan ADCs لدينا إضافة رائعة إلى محفظتك. نحن دائمًا منفتحون على المناقشات حول كيفية ملاءمة منتجاتنا مع خطط البحث أو العلاج.
إذا كنت مهتمًا بمعرفة المزيد عن أدوية Deruxtecan Adibody المترافق أو ترغب في بدء محادثة حول المشتريات ، فلا تتردد في التواصل. نحن هنا للإجابة على أسئلتك ومساعدتك على أخذ بحث أو ممارسة علاج السرطان إلى المستوى التالي.
مراجع
- كارتر ، PJ ، & Senter ، PD (2008). الأجسام المضادة - مقارنات المخدرات لعلاج السرطان. مجلة السرطان ، 14 (3) ، 154 - 169.
- Modi ، S. ، et al. (2020). Trastuzumab deruxtecan في سرطان الثدي النقيلي الإيجابي النقيلي. مجلة نيو إنجلاند للطب ، 382 (7) ، 610 - 621.
- Sliwkowski ، MX ، & Mellman ، I. (2013). الأجسام المضادة - مقارنات المخدرات: تقدم Armamentarium السرطان. الطب العلمي للطب ، 5 (209) ، 209RV13.
